Une technologie révolutionnaire révèle les secrets du « retour en arrière » dans la régulation des gènes
[ad_1]
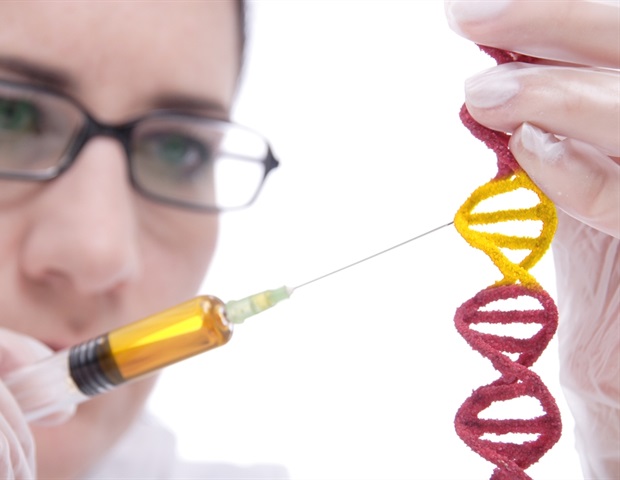
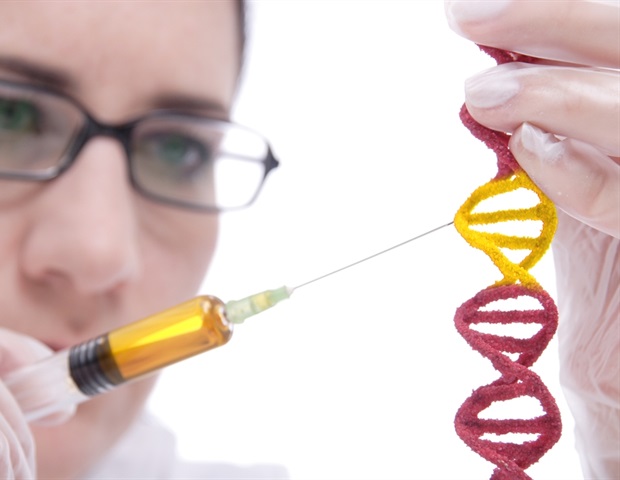
Une nouvelle étude montre qu’une technique peut, pour la première fois, déterminer la fréquence et l’endroit précis où un événement moléculaire appelé « retour en arrière » se produit dans le matériel génétique d’une espèce (génome).
Publié en ligne le 9 février dans cellule moléculaire, Les résultats de l’étude soutiennent la théorie selon laquelle le retour en arrière représente une forme répandue de régulation génétique qui affecte des milliers de gènes humains, dont beaucoup sont impliqués dans des processus vitaux fondamentaux tels que la division cellulaire et le développement dans l’utérus.
Dirigés par des chercheurs de la Grossman School of Medicine de NYU, les travaux tournent autour des gènes, les sections de « lettres » moléculaires de l’ADN disposées dans un ordre (séquence) spécifique pour coder les plans de la plupart des organismes. Chez les humains comme chez les bactéries, la première étape de l’expression d’un gène, la transcription, se produit sous la forme d’une « machine » protéique appelée ARN polymérase II, qui parcourt la chaîne d’ADN et lit les instructions génétiques dans une direction.
En 1997, le Dr. Evgeny Nudler et ses collègues ont publié un article montrant que l’ARN polymérase peut parfois reculer le long de la chaîne qu’elle lit, un phénomène qu’ils ont appelé « retour en arrière ». Depuis lors, des études ont montré que dans les cellules vivantes, un retour en arrière se produit parfois peu de temps après que l’ARN polymérase commence à synthétiser l’ARN ou lorsqu’elle rencontre de l’ADN endommagé pour faire place aux enzymes de réparation entrantes. Des travaux ultérieurs ont suggéré que les mécanismes de rechute et de réparation devaient fonctionner rapidement et se désintégrer, sinon ils pourraient entrer en collision avec l’ADN polymérase et provoquer la mort cellulaire, provoquant des ruptures des chaînes d’ADN.
Maintenant, une nouvelle étude de l’équipe de Nudler à NYU Langone Health montre que leur nouvelle technique, le séquençage de clivage à longue portée (LORAX-seq), peut détecter directement où commencent et se terminent les événements de retour en arrière. En complétant les approches précédentes indirectes ou limitées, la nouvelle méthode montre que de nombreux événements de ce type remontent plus loin qu’on ne le pensait et durent donc plus longtemps. Les résultats suggèrent également qu’un retour en arrière persistant se produit fréquemment dans tout le génome, se produit plus fréquemment à proximité de types de gènes spécifiques et a des fonctions bien au-delà de la réparation de l’ADN.
La stabilité surprenante du retour en arrière sur de plus longues distances laisse penser qu’il s’agit d’une forme omniprésente de régulation génétique chez des espèces allant des bactéries aux humains. Si d’autres travaux étendent nos découvertes à divers programmes de développement et conditions pathologiques, le retour en arrière pourrait ressembler à l’épigénétique, dont la découverte a révélé un nouveau niveau surprenant de régulation génique sans altérer le code ADN.
Evgeny Nudler, PhD, auteur principal de l’étude et professeur Julie Wilson Anderson au Département de biochimie et de pharmacologie moléculaire de NYU Langone
Au centre de la vie ?
L’ARN polymérase II traduit le code de l’ADN en un matériau connexe appelé ARN, qui dirige ensuite la construction des protéines. Pour ce faire, le complexe se déplace dans une direction le long des chaînes d’ADN, mais revient dans certains scénarios. Des études antérieures ont montré qu’à mesure que l’ARN polymérase II recule, elle pousse (extrude) la pointe de la chaîne d’ARN qu’elle a construite à partir du code ADN hors de son canal interne. Étant donné qu’un retour en arrière prolongé peut conduire à des collisions dommageables, on pense que la transcription est rapidement restaurée par le facteur de transcription IIS (TFIIS), qui favorise la troncature (clivage) de l’ARN extrudé et « revenu en arrière ». Cela ouvre la voie à l’ARN polymérase II pour continuer à lire le code direct.
Cependant, d’autres études antérieures avaient montré que l’ARN tracé pouvait s’attacher au canal à travers lequel il est extrudé et le maintenir en place plus longtemps lorsque la polymérase parcourt une certaine distance (par exemple 20 éléments constitutifs de l’ADN de nucléobases). Les complexes de retracement bloqués sont moins susceptibles d’être sauvés par le clivage dirigé par TFIIS et plus susceptibles de retarder la transcription du gène impliqué. Cela a conduit à la théorie selon laquelle le retour en arrière joue non seulement un rôle clé dans les voies de réparation de l’ADN, mais pourrait également augmenter ou diminuer l’effet des gènes en tant que mécanisme de régulation important.
Selon les chercheurs, le TFIIS est probablement présent à de faibles niveaux dans les cellules vivantes et entre en compétition avec des centaines d’autres protéines pour accéder et exciser l’ARN tracé afin que la transcription puisse se poursuivre. Dans la présente étude, l’équipe a plutôt utilisé une forte concentration de TFIIS purifié (sans protéines concurrentes) pour exciser avec précision chaque morceau d’ARN tracé partout où il se trouve dans le code génétique d’une cellule. Cela a rendu les extraits coupés accessibles aux technologies qui lisent les séquences de code et fournissent des indices sur leur emplacement et leur fonction.
L’équipe de recherche a également découvert que les gènes qui contrôlent les histones – des « bobines » de protéines autour desquelles les chaînes d’ADN s’enroulent dans la chromatine qui organise l’expression des gènes – sont très vulnérables à un retour en arrière prolongé. Les auteurs émettent l’hypothèse que la mesure dans laquelle cela se produit, ainsi que les changements associés dans la transcription de certains gènes, pourraient contrôler le moment de l’accumulation d’histones à grande échelle, nécessaire à la reconstruction de la chromatine au cours de la division cellulaire. Ils suggèrent également qu’un retour en arrière soutenu pourrait affecter la transcription en temps opportun de gènes importants pour le développement des tissus.
“En plus de ses fonctions potentiellement utiles, un retour en arrière persistant pourrait également conduire à des dommages à l’ADN et à d’autres dysfonctionnements génétiques qui contribuent à la maladie”, explique l’auteur principal de l’étude, Kevin Yang, étudiant diplômé du Dr. Le laboratoire de Nudler. « Nous pensons que mesurer le retour en arrière dans le contexte du vieillissement ou du cancer, par exemple, pourrait nous aider à comprendre pourquoi des dysfonctionnements dans la réponse cellulaire au stress et la réplication cellulaire se produisent et suggérer de nouvelles approches thérapeutiques. »
Outre Yang et Nudler, les auteurs de l’étude du Département de biochimie et de pharmacologie moléculaire de NYU Langone Health comprenaient Aviram Rasouly, Vitaly Epshtein, Criseyda Martinez, Thao Nguyen et Ilya Shamovsky. Nudler est également chercheur au Howard Hughes Medical Institute. L’étude est financée par la Blavatnik Family Foundation, le Howard Hughes Medical Institute et les subventions R01GM126891 et T32 AI007180 des National Institutes of Health.
Source:
Référence du magazine :
Yang, KB, et autres. (2024). Persistance du retour en arrière par l’ARN polymérase II humaine. Cellule moléculaire. doi.org/10.1016/j.molcel.2024.01.019.
[ad_2]
Source
